

Saccharide sind die am häufigsten vorkommenden organischen Substanzen in der Natur und lebensnotwendig. Das Verständnis, wie Kohlenhydrate Proteine während physiologischer und pathologischer Prozesse regulieren, kann Möglichkeiten bieten, wichtige biologische Fragen zu beantworten und neue Behandlungen zu entwickeln.
Allerdings stellt die Vielfalt und Komplexität der Zuckermoleküle eine Herausforderung dar, die Bindungs- und Interaktionsstellen zwischen Zucker und Protein experimentell zu identifizieren.
Hier hat ein Team der Chinesischen Akademie der Wissenschaften DeepGlycanSite entwickelt, ein Deep-Learning-Modell, das in der Lage ist, Zuckerbindungsstellen auf einer bestimmten Proteinstruktur genau vorherzusagen.
DeepGlycanSite integriert die geometrischen und evolutionären Eigenschaften von Proteinen in ein tiefes äquivariantes graphisches neuronales Netzwerk mit einer Transformer-Architektur. Seine Leistung übertrifft frühere fortschrittliche Methoden deutlich und kann die Bindungsstellen verschiedener Zuckermoleküle effektiv vorhersagen.
In Kombination mit Mutagenesestudien deckt DeepGlycanSite die Guanosin-5'-bisphosphat-Erkennungsstelle wichtiger G-Protein-gekoppelter Rezeptoren auf.
Diese Ergebnisse zeigen den Wert von DeepGlycanSite für die Vorhersage von Zuckerbindungsstellen und können Einblicke in die molekularen Mechanismen hinter der Zuckerregulation von Proteinen von therapeutischer Bedeutung liefern.
Die Studie trug den Titel „Hochpräzise Vorhersage der Kohlenhydratbindungsstelle mit DeepGlycanSite“ und wurde am 17. Juni 2024 in „Nature Communications“ veröffentlicht.

Zucker ist auf der Zelloberfläche aller Organismen allgegenwärtig. Sie interagieren mit einer Vielzahl von Proteinfamilien wie Lektinen, Antikörpern, Enzymen und Transportern, um wichtige biologische Prozesse wie Immunantwort, Zelldifferenzierung und Nervenentwicklung zu regulieren. Das Verständnis des Wechselwirkungsmechanismus zwischen Kohlenhydraten und Proteinen ist die Grundlage für die Entwicklung von Kohlenhydrat-Medikamenten.
Die Vielfalt und Komplexität der Kohlenhydratstrukturen, insbesondere die Variabilität ihrer Bindungsstellen mit Proteinen, stellen jedoch die Erfassung experimenteller Daten und das Arzneimitteldesign vor Herausforderungen. Abbildung: Die Komplexität von Zuckermolekülen und die Vielfalt der Zuckerbindungsstellen. (Quelle: Papier)
 In der Vergangenheit waren herkömmliche Methoden zur Vorhersage von Bindungsstellen nicht für Zuckermoleküle mit komplexen Strukturen und großen Größenänderungen geeignet. In Kombination mit dem Mangel an hochauflösenden Strukturdaten des Zucker-Protein-Komplexes schränkt dies die Leistung von Vorhersagemodellen ein.
In der Vergangenheit waren herkömmliche Methoden zur Vorhersage von Bindungsstellen nicht für Zuckermoleküle mit komplexen Strukturen und großen Größenänderungen geeignet. In Kombination mit dem Mangel an hochauflösenden Strukturdaten des Zucker-Protein-Komplexes schränkt dies die Leistung von Vorhersagemodellen ein.
In den letzten Jahren hat die akademische Gemeinschaft mit der rasanten Entwicklung der Proteindatenbank (PDB) und offenen Glykomik-Ressourcen Strukturdaten von mehr als 19.000 solcher Komplexe gesammelt. Die Zunahme dieser hochwertigen Daten ermöglicht den Einsatz von KI-Technologie zur Entwicklung genauer Modelle zur Vorhersage von Zuckerbindungsstellen, was den Entdeckungs- und Optimierungsprozess von Zuckermedikamenten beschleunigen dürfte. In der neuesten Forschung stellte das Team der Chinesischen Akademie der Wissenschaften DeepGlycanSite vor, ein EGNN-Modell (Deep Equivariant Graph Neural Network), das Zuckerbindungsstellen mit Zielproteinstrukturen genau vorhersagen kann.
Abbildung: DeepGlycanSite-Übersicht. (Quelle: Papier)
 Das Team nutzte geometrische Merkmale wie Richtungen und Abstände innerhalb und zwischen Resten sowie evolutionäre Informationen, um Proteine als grafische Darstellungen auf Restebene in DeepGlycanSite darzustellen. Kombiniert mit Transformer-Blöcken mit Selbstaufmerksamkeitsmechanismus zur Verbesserung der Merkmalsextraktion und der Erkennung komplexer Beziehungen.
Das Team nutzte geometrische Merkmale wie Richtungen und Abstände innerhalb und zwischen Resten sowie evolutionäre Informationen, um Proteine als grafische Darstellungen auf Restebene in DeepGlycanSite darzustellen. Kombiniert mit Transformer-Blöcken mit Selbstaufmerksamkeitsmechanismus zur Verbesserung der Merkmalsextraktion und der Erkennung komplexer Beziehungen.
Forscher verglichen DeepGlycanSite mit aktuellen, hochmodernen Berechnungsmethoden anhand eines unabhängigen Testsatzes mit mehr als hundert einzigartigen zuckerbindenden Proteinen. Die Ergebnisse zeigen, dass der durchschnittliche Matthews-Korrelationskoeffizient (MCC) von DeepGlycanSite (0,625) mehr als das 30-fache des von StackCBPred (0,018) beträgt und andere sequenzbasierte Vorhersagemethoden bei weitem übertrifft.
Herkömmliche Methoden zur Ligandenbindungsstelle können Bindungsstellen für einfache Zuckermoleküle aufgrund ihrer Hydrophobie oder geringen Größe ausschließen, während DeepGlycanSite diese Stellen effektiv identifizieren kann.在-Symbol: Vergleichen Sie Modelle, um die Leistung verschiedener Zuckerbindungsstellen vorherzusagen. (Quelle: Papier)
Darüber hinaus leistet DeepGlycanSite auch gute Ergebnisse bei der Vorhersage mehrerer Zuckerbindungsstellen auf Proteinen, was von großem Wert für das Verständnis ist, wie multivalente Glykokonjugate Zucker-Protein-Wechselwirkungen und die Regulierung biologischer Prozesse beeinflussen. Beispielsweise werden multivalente Glykokonjugate als chemische Werkzeuge und Wirkstoffkandidaten entwickelt, um die Wechselwirkung zwischen Zuckermolekülen und Lektinen zu beeinflussen.
Im Gegensatz zu herkömmlichen Methoden, die nur Proteinsequenz- oder Strukturinformationen verwenden, berücksichtigt DeepGlycanSite vollständig die geometrischen Informationen und evolutionären Eigenschaften des Proteins, die ein Schlüsselfaktor für seine hervorragende Leistung sein können.
Darüber hinaus kann DeepGlycanSite anhand der chemischen Struktur eines abgefragten Zuckermoleküls dessen spezifische Bindungsstelle vorhersagen.的-Symbol: Abfrage der spezifischen Bindungsstellenvorhersage von Zucker. (Quelle: Papier)
 Forscher untersuchten die Anwendung von DeepGlycanSite auf funktionell wichtige G-Protein-gekoppelte Rezeptoren (GPCRs). Mithilfe der von AlphaFold2 vorhergesagten Proteinstruktur und chemischen Kohlenhydratstruktur konnte DeepGlycanSite erfolgreich die spezifische Bindungsstelle von GDP-Fuc auf menschlichem P2Y14 nachweisen. Abbildung: Experimentelle Verifizierung von DeepGlycanSite. (Quelle: Paper)
Forscher untersuchten die Anwendung von DeepGlycanSite auf funktionell wichtige G-Protein-gekoppelte Rezeptoren (GPCRs). Mithilfe der von AlphaFold2 vorhergesagten Proteinstruktur und chemischen Kohlenhydratstruktur konnte DeepGlycanSite erfolgreich die spezifische Bindungsstelle von GDP-Fuc auf menschlichem P2Y14 nachweisen. Abbildung: Experimentelle Verifizierung von DeepGlycanSite. (Quelle: Paper)
Während die Qualität der Seitenkettenvorhersagen von AlphaFold2 verbessert werden könnte, ist DeepGlycanSite weniger auf die Genauigkeit der Proteinstruktur angewiesen und ist in der Lage, vorhergesagte Proteinstrukturen zu verwenden, um Einblicke in Zucker-Protein-Wechselwirkungen zu liefern.
Zusammenfassend zeigt die Validierung von DeepGlycanSite in unabhängigen Testreihen und In-vitro-Fallstudien, dass es ein wirksames Werkzeug zur Vorhersage von Zuckerbindungsstellen ist. Forscher können DeepGlycanSite verwenden, um Zuckerbindungstaschen auf Zielproteinen vorherzusagen und so das Verständnis der Zucker-Protein-Wechselwirkungen zu verbessern. Saccharide spielen eine Schlüsselrolle bei biologischen Funktionen. DeepGlycanSite hilft nicht nur bei der Analyse der biologischen Funktionen von Zuckermolekülen und zuckerbindenden Proteinen, sondern bietet auch ein leistungsstarkes Werkzeug für die Entwicklung von Zuckermedikamenten.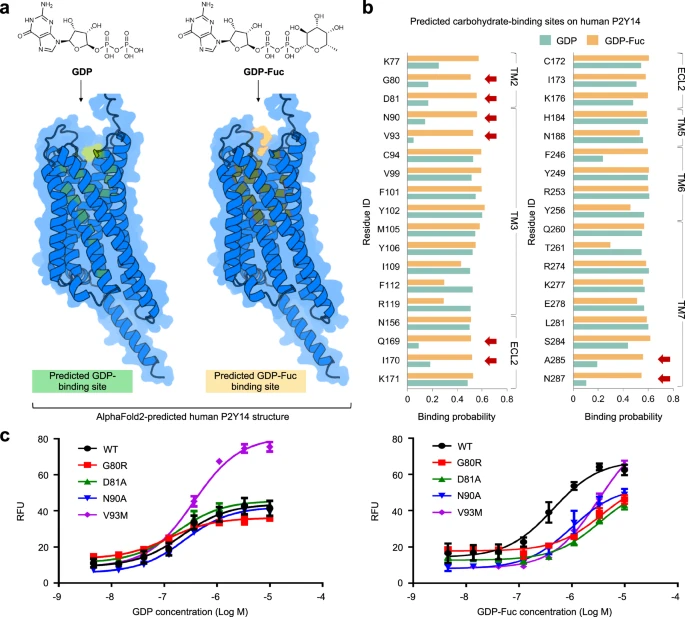
Das obige ist der detaillierte Inhalt vonDas Transformer-Deep-Learning-Modell des Teams der Chinesischen Akademie der Wissenschaften ist 30-mal effizienter als herkömmliche Methoden und sagt die Interaktionsorte zwischen Zucker und Protein voraus. Für weitere Informationen folgen Sie bitte anderen verwandten Artikeln auf der PHP chinesischen Website!
 Die heutige Toutiao-Goldmünze entspricht 1 Yuan
Die heutige Toutiao-Goldmünze entspricht 1 Yuan
 Was sind die kostenlosen virtuellen PHP-Hosts im Ausland?
Was sind die kostenlosen virtuellen PHP-Hosts im Ausland?
 So laden Sie den Razer-Maustreiber herunter
So laden Sie den Razer-Maustreiber herunter
 So beheben Sie einen Analysefehler
So beheben Sie einen Analysefehler
 Assoziationsregeln Apriori-Algorithmus
Assoziationsregeln Apriori-Algorithmus
 Zellsumme
Zellsumme
 Wie viele Menschen können Sie mit Douyin großziehen?
Wie viele Menschen können Sie mit Douyin großziehen?
 C-Sprache, sonst Verwendung der if-Anweisung
C-Sprache, sonst Verwendung der if-Anweisung




