Technologie-Peripheriegeräte
Technologie-Peripheriegeräte
 KI
KI
 SOTA Performance, eine multimodale KI-Methode zur Vorhersage der Protein-Ligand-Affinität in Xiamen, kombiniert erstmals molekulare Oberflächeninformationen
SOTA Performance, eine multimodale KI-Methode zur Vorhersage der Protein-Ligand-Affinität in Xiamen, kombiniert erstmals molekulare Oberflächeninformationen
SOTA Performance, eine multimodale KI-Methode zur Vorhersage der Protein-Ligand-Affinität in Xiamen, kombiniert erstmals molekulare Oberflächeninformationen

Herausgeber |. KX
Im Bereich der Arzneimittelforschung und -entwicklung ist die genaue und effektive Vorhersage der Bindungsaffinität von Proteinen und Liganden für das Arzneimittelscreening und die Arzneimitteloptimierung von entscheidender Bedeutung. Aktuelle Studien berücksichtigen jedoch nicht die wichtige Rolle molekularer Oberflächeninformationen bei Protein-Ligand-Wechselwirkungen.
Auf dieser Grundlage schlugen Forscher der Universität Xiamen ein neuartiges MFE-Framework (Multimodal Feature Extraction) vor, das erstmals Informationen über Proteinoberfläche, 3D-Struktur und -Sequenz kombiniert und einen Kreuzaufmerksamkeitsmechanismus für verschiedene Modi verwendet. Feature-Ausrichtung zwischen Staaten.
Experimentelle Ergebnisse zeigen, dass diese Methode bei der Vorhersage der Protein-Ligand-Bindungsaffinität Spitzenleistungen erbringt. Darüber hinaus belegen Ablationsstudien die Wirksamkeit und Notwendigkeit der Proteinoberflächeninformation und der multimodalen Merkmalsausrichtung innerhalb dieses Rahmens.
Verwandte Forschung mit dem Titel „Oberflächenbasierte multimodale Protein-Ligand-Bindungsaffinitätsvorhersage“ wurde am 21. Juni auf „Bioinformatik“ veröffentlicht.

Forschung zur Vorhersage der Protein-Ligand-Bindungsaffinität
Als Schlüsselphase der Arzneimittelentwicklung wird die Vorhersage der Protein-Ligand-Bindungsaffinität seit langem ausführlich untersucht, was für ein effizientes und genaues Arzneimittelscreening von entscheidender Bedeutung ist.
Herkömmliche computergestützte Tools zur Arzneimittelentdeckung nutzen Scoring-Funktionen (SF), um die Protein-Ligand-Bindungsaffinität grob abzuschätzen, jedoch mit geringer Genauigkeit. Molekulardynamik-Simulationsmethoden können genauere Schätzungen der Bindungsaffinität liefern, sind jedoch oft kostspielig und zeitaufwändig.
Mit der Entwicklung der Computertechnologie und der zunehmenden Fülle umfangreicher biologischer Daten haben Deep-Learning-basierte Methoden großes Potenzial im Bereich der Vorhersage der Protein-Ligand-Bindungsaffinität gezeigt.
Allerdings nutzt die aktuelle Forschung hauptsächlich sequenz- oder strukturbasierte Darstellungen, um die Protein-Ligand-Bindungsaffinität vorherzusagen, und es gibt relativ wenige Studien zu Proteinoberflächeninformationen, die für Protein-Ligand-Wechselwirkungen entscheidend sind.
Eine molekulare Oberfläche ist eine hochrangige Darstellung der Struktur eines Proteins, die charakteristische chemische und geometrische Muster aufweist, die als Fingerabdrücke der Interaktionsmuster des Proteins mit anderen Biomolekülen dienen. Daher begannen einige Studien, Proteinoberflächeninformationen zu nutzen, um die Protein-Ligand-Bindungsaffinität vorherzusagen.
Aber bestehende Methoden konzentrieren sich hauptsächlich auf monomodale Daten und ignorieren die multimodalen Informationen von Proteinen. Darüber hinaus verbinden herkömmliche Methoden bei der Verarbeitung multimodaler Informationen von Proteinen normalerweise Merkmale verschiedener Modalitäten direkt, ohne die Heterogenität zwischen ihnen zu berücksichtigen, was dazu führt, dass die Komplementarität zwischen Modalitäten nicht effektiv genutzt werden kann.
Neuartiges Framework zur multimodalen Merkmalsextraktion
Hier schlagen Forscher ein neuartiges Framework zur multimodalen Merkmalsextraktion (MFE) vor, das zum ersten Mal Informationen aus Proteinoberfläche, 3D-Struktur und Sequenz kombiniert.
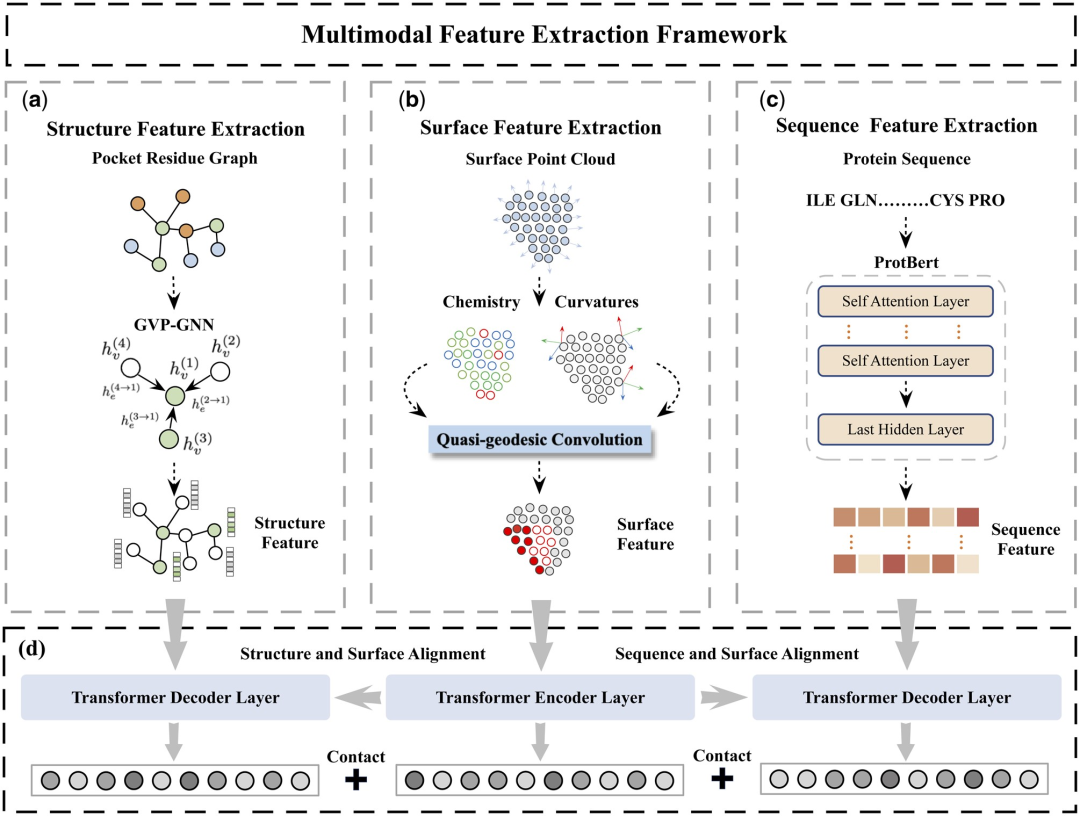
Konkret wurden in der Studie zwei Hauptkomponenten entworfen: das Protein-Merkmalsextraktionsmodul und das multimodale Merkmalsvergleichsmodul.
Das Protein-Feature-Extraktionsmodul wird verwendet, um anfängliche Einbettungen aus Proteinoberflächen-, Struktur- und Sequenzinformationen zu extrahieren.
Im multimodalen Merkmalsvergleichsmodul wird der Kreuzaufmerksamkeitsmechanismus verwendet, um einen Merkmalsvergleich zwischen Proteinstruktur, Sequenzeinbettung und Oberflächeneinbettung zu erreichen und so eine einheitliche und informationsreiche Merkmalseinbettung zu erhalten.
Im Vergleich zu aktuellen Methoden auf dem neuesten Stand der Technik erzielt das vorgeschlagene Framework die besten Ergebnisse bei der Aufgabe der Vorhersage der Protein-Ligand-Bindungsaffinität.
SOTA-Leistung
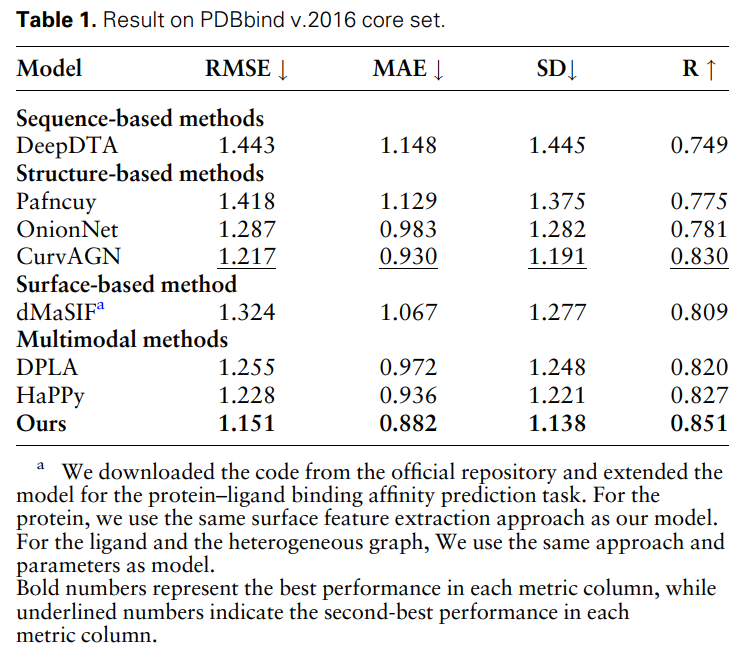
Tabelle 1 zeigt die Ergebnisse von MFE und anderen Basismodellen zur Vorhersage der Protein-Ligand-Bindungsaffinität. Alle Modelle verwendeten die gleiche Partitionierungsmethode für Trainings- und Validierungssätze und wurden auf dem PDBbind-Kernsatz (Version 2016) getestet. Es kann festgestellt werden, dass die MFE-Methode im Vergleich zu allen Basislinien eine SOTA-Leistung erzielt.
Ablationsstudie
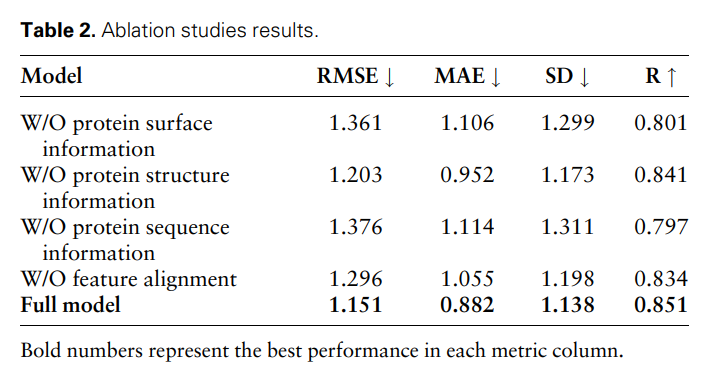
Um die Wirksamkeit und Notwendigkeit verschiedener modaler Merkmale und Merkmalsvergleiche weiter zu beweisen, führten die Forscher die folgenden Ablationsstudien durch: Informationen zur W/O-Proteinoberfläche, Informationen zur W/O-Proteinstruktur, w/ o Proteinsequenzinformationen und merkmalslose Alignments. Die Ergebnisse sind in Tabelle 2 und Abbildung 2 dargestellt.
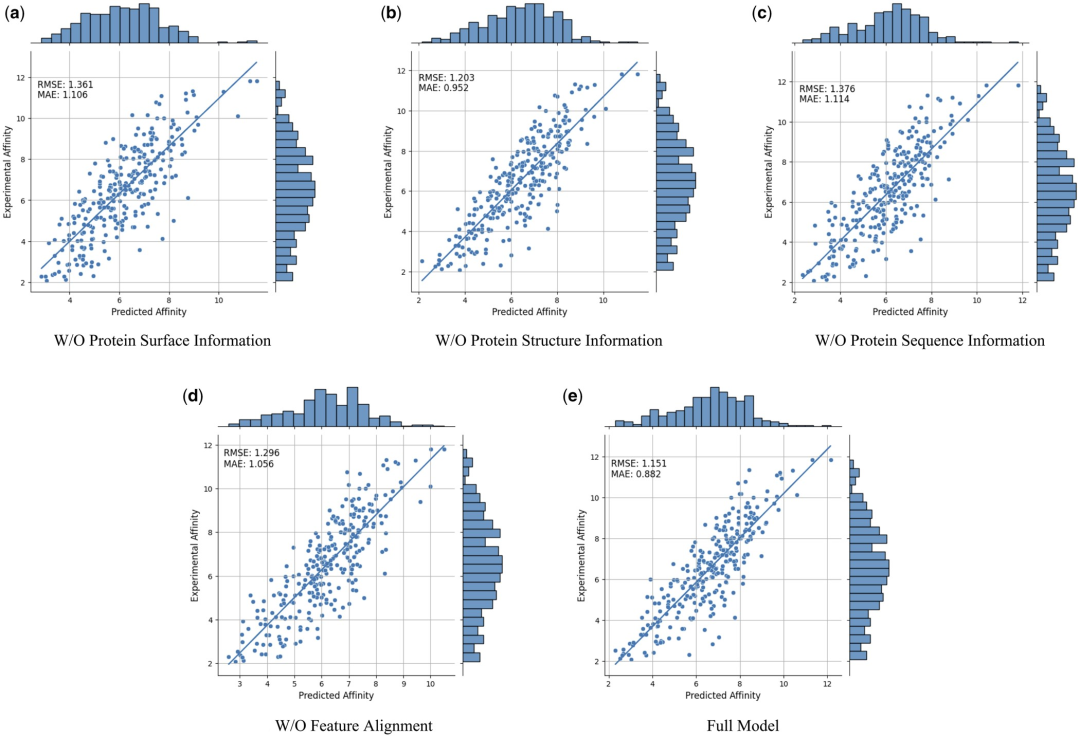
Abbildung 2: Ergebnisse der Ablationsstudie. (Quelle: Papier)
Die Ergebnisse zeigen, dass die Leistung erheblich abnimmt, wenn Oberflächeninformationen entfernt werden, was darauf hindeutet, dass Oberflächeninformationen eine entscheidende Rolle im Modell spielen. Ebenso führt der Ausschluss von Struktur- oder Sequenzinformationen zu einer Leistungsverschlechterung, während die Eliminierung von Sequenzinformationen zu einer stärkeren Verschlechterung führt. Dies liegt daran, dass Sequenzinformationen globale Informationen über das Protein enthalten, die für das vollständige Verständnis des Proteins durch das Modell von entscheidender Bedeutung sind.
Darüber hinaus nimmt ohne Funktionsvergleich die Leistung des Modells ab. Dies unterstreicht die Bedeutung des Merkmalsvergleichs bei der Verarbeitung multimodaler Daten, da er dazu beiträgt, die Heterogenität zwischen verschiedenen Modalmerkmalen zu verringern und dadurch die Fähigkeit des Modells zur effektiven Integration verschiedener Modalmerkmale zu verbessern.
Hyperparameteranalyse
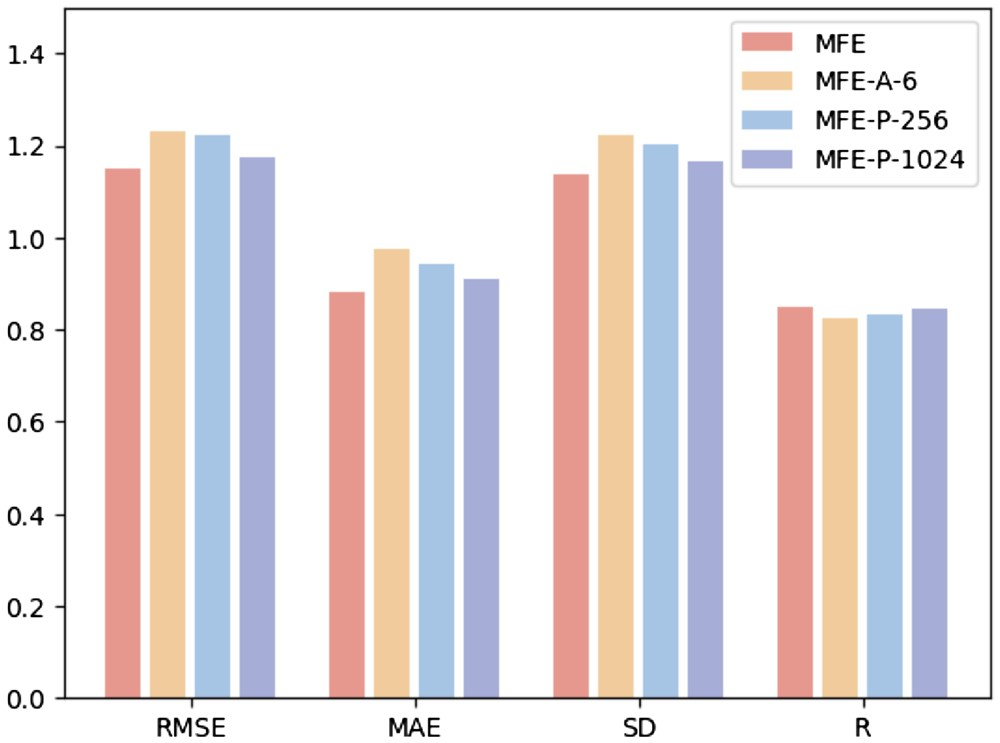
Um den Einfluss verschiedener Hyperparameter auf die Modellleistung zu untersuchen, führten die Forscher die folgenden drei Experimente durch: (i) MFE-A-6: Verwenden Sie nur 6 grundlegende Atomtypen zur Darstellung von Chemikalien Eigenschaften der Oberfläche, einschließlich Wasserstoff, Kohlenstoff, Stickstoff, Sauerstoff, Phosphor und Schwefel; (ii) MFE-P-256: Nur die 256 Oberflächenpunkte, die dem Ligandenzentrum am nächsten liegen, werden als Proteintaschenoberfläche ausgewählt; -P -1024: Wählen Sie die 1024 Oberflächenpunkte, die dem Ligandenzentrum am nächsten liegen, als Proteintaschenoberfläche aus.
Abbildung 3 zeigt die Ergebnisse von drei verschiedenen Hyperparameter-Auswahlmethoden für die Aufgabe zur Vorhersage der Protein-Ligand-Bindungsaffinität.
Merkmalsausrichtungsanalyse und -visualisierung
Um den Einfluss der Merkmalsausrichtung auf die Modellleistung eingehend zu untersuchen, verwendeten die Forscher die Hauptkomponentenanalyse (PCA), um eine Dimensionsreduktion und Summierung der Proteinoberfläche und -struktur durchzuführen und Sequenzmerkmale im Testsatz Visuelle Analyse. Mit diesem Ansatz soll ermittelt werden, ob die Merkmalsausrichtung die Heterogenität zwischen multimodalen Einbettungen verringern kann.
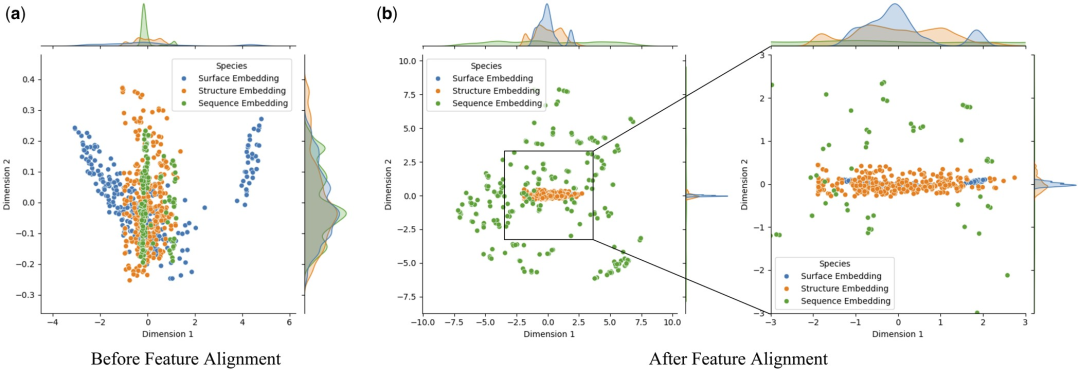
Untersuchungen haben ergeben, dass die Merkmalsausrichtung die Konsistenz zwischen Proteinoberfläche, Struktur und Sequenzeinbettung deutlich verbessert. Dies ist auf die Optimierung multimodaler Feature-Interaktionen in Transformer durch den Aufmerksamkeitsmechanismus zurückzuführen, der Aufmerksamkeitsgewichte zwischen verschiedenen Features berechnet. Dies verbessert die Fähigkeit des Modells, wichtige Informationen zu erfassen, wodurch Daten aus verschiedenen Modalitäten enger im Merkmalsraum geclustert werden können, wodurch Rauschen und Fehler bei der Identifizierung von Protein-Ligand-Wechselwirkungen durch das Modell reduziert werden.
Abschließend kamen die Forscher zu dem Schluss: „Zusammenfassend können wir durch die Untersuchung der Oberfläche von Proteinen ein tieferes Verständnis dafür erlangen, wie Proteine mit anderen Biomolekülen interagieren. In zukünftigen Arbeiten werden wir Proteinoberflächen gründlicher untersuchen, um ihre breitere Anwendung aufzudecken.“ Bioinformatik“
Hinweis: Das Cover stammt aus dem Internet
.Das obige ist der detaillierte Inhalt vonSOTA Performance, eine multimodale KI-Methode zur Vorhersage der Protein-Ligand-Affinität in Xiamen, kombiniert erstmals molekulare Oberflächeninformationen. Für weitere Informationen folgen Sie bitte anderen verwandten Artikeln auf der PHP chinesischen Website!

Heiße KI -Werkzeuge
Undresser.AI Undress
KI-gestützte App zum Erstellen realistischer Aktfotos
AI Clothes Remover
Online-KI-Tool zum Entfernen von Kleidung aus Fotos.

Undress AI Tool
Ausziehbilder kostenlos

Clothoff.io
KI-Kleiderentferner
Video Face Swap
Tauschen Sie Gesichter in jedem Video mühelos mit unserem völlig kostenlosen KI-Gesichtstausch-Tool aus!

Heißer Artikel

Heiße Werkzeuge

Notepad++7.3.1
Einfach zu bedienender und kostenloser Code-Editor

SublimeText3 chinesische Version
Chinesische Version, sehr einfach zu bedienen

Senden Sie Studio 13.0.1
Leistungsstarke integrierte PHP-Entwicklungsumgebung

Dreamweaver CS6
Visuelle Webentwicklungstools

SublimeText3 Mac-Version
Codebearbeitungssoftware auf Gottesniveau (SublimeText3)

Heiße Themen
 1669
1669
 14
14
 1428
1428
 52
52
 1329
1329
 25
25
 1273
1273
 29
29
 1256
1256
 24
24
 Bytedance Cutting führt SVIP-Supermitgliedschaft ein: 499 Yuan für ein fortlaufendes Jahresabonnement, das eine Vielzahl von KI-Funktionen bietet
Jun 28, 2024 am 03:51 AM
Bytedance Cutting führt SVIP-Supermitgliedschaft ein: 499 Yuan für ein fortlaufendes Jahresabonnement, das eine Vielzahl von KI-Funktionen bietet
Jun 28, 2024 am 03:51 AM
Diese Seite berichtete am 27. Juni, dass Jianying eine von FaceMeng Technology, einer Tochtergesellschaft von ByteDance, entwickelte Videobearbeitungssoftware ist, die auf der Douyin-Plattform basiert und grundsätzlich kurze Videoinhalte für Benutzer der Plattform produziert Windows, MacOS und andere Betriebssysteme. Jianying kündigte offiziell die Aktualisierung seines Mitgliedschaftssystems an und führte ein neues SVIP ein, das eine Vielzahl von KI-Schwarztechnologien umfasst, wie z. B. intelligente Übersetzung, intelligente Hervorhebung, intelligente Verpackung, digitale menschliche Synthese usw. Preislich beträgt die monatliche Gebühr für das Clipping von SVIP 79 Yuan, die Jahresgebühr 599 Yuan (Hinweis auf dieser Website: entspricht 49,9 Yuan pro Monat), das fortlaufende Monatsabonnement beträgt 59 Yuan pro Monat und das fortlaufende Jahresabonnement beträgt 499 Yuan pro Jahr (entspricht 41,6 Yuan pro Monat). Darüber hinaus erklärte der Cut-Beamte auch, dass diejenigen, die den ursprünglichen VIP abonniert haben, das Benutzererlebnis verbessern sollen
 „Defect Spectrum' durchbricht die Grenzen der herkömmlichen Fehlererkennung und erreicht erstmals eine hochpräzise und umfassende semantische Fehlererkennung in der Industrie.
Jul 26, 2024 pm 05:38 PM
„Defect Spectrum' durchbricht die Grenzen der herkömmlichen Fehlererkennung und erreicht erstmals eine hochpräzise und umfassende semantische Fehlererkennung in der Industrie.
Jul 26, 2024 pm 05:38 PM
In der modernen Fertigung ist die genaue Fehlererkennung nicht nur der Schlüssel zur Sicherstellung der Produktqualität, sondern auch der Kern für die Verbesserung der Produktionseffizienz. Allerdings mangelt es vorhandenen Datensätzen zur Fehlererkennung häufig an der Genauigkeit und dem semantischen Reichtum, die für praktische Anwendungen erforderlich sind, was dazu führt, dass Modelle bestimmte Fehlerkategorien oder -orte nicht identifizieren können. Um dieses Problem zu lösen, hat ein Spitzenforschungsteam bestehend aus der Hong Kong University of Science and Technology Guangzhou und Simou Technology innovativ den „DefectSpectrum“-Datensatz entwickelt, der eine detaillierte und semantisch reichhaltige groß angelegte Annotation von Industriedefekten ermöglicht. Wie in Tabelle 1 gezeigt, bietet der Datensatz „DefectSpectrum“ im Vergleich zu anderen Industriedatensätzen die meisten Fehleranmerkungen (5438 Fehlerproben) und die detaillierteste Fehlerklassifizierung (125 Fehlerkategorien).
 Training mit Millionen von Kristalldaten zur Lösung kristallographischer Phasenprobleme, die Deep-Learning-Methode PhAI wird in Science veröffentlicht
Aug 08, 2024 pm 09:22 PM
Training mit Millionen von Kristalldaten zur Lösung kristallographischer Phasenprobleme, die Deep-Learning-Methode PhAI wird in Science veröffentlicht
Aug 08, 2024 pm 09:22 PM
Herausgeber |KX Bis heute sind die durch die Kristallographie ermittelten Strukturdetails und Präzision, von einfachen Metallen bis hin zu großen Membranproteinen, mit keiner anderen Methode zu erreichen. Die größte Herausforderung, das sogenannte Phasenproblem, bleibt jedoch die Gewinnung von Phaseninformationen aus experimentell bestimmten Amplituden. Forscher der Universität Kopenhagen in Dänemark haben eine Deep-Learning-Methode namens PhAI entwickelt, um Kristallphasenprobleme zu lösen. Ein Deep-Learning-Neuronales Netzwerk, das mithilfe von Millionen künstlicher Kristallstrukturen und den entsprechenden synthetischen Beugungsdaten trainiert wird, kann genaue Elektronendichtekarten erstellen. Die Studie zeigt, dass diese Deep-Learning-basierte Ab-initio-Strukturlösungsmethode das Phasenproblem mit einer Auflösung von nur 2 Angström lösen kann, was nur 10 bis 20 % der bei atomarer Auflösung verfügbaren Daten im Vergleich zur herkömmlichen Ab-initio-Berechnung entspricht
 Das NVIDIA-Dialogmodell ChatQA wurde auf Version 2.0 weiterentwickelt, wobei die angegebene Kontextlänge 128 KB beträgt
Jul 26, 2024 am 08:40 AM
Das NVIDIA-Dialogmodell ChatQA wurde auf Version 2.0 weiterentwickelt, wobei die angegebene Kontextlänge 128 KB beträgt
Jul 26, 2024 am 08:40 AM
Die offene LLM-Community ist eine Ära, in der hundert Blumen blühen und konkurrieren. Sie können Llama-3-70B-Instruct, QWen2-72B-Instruct, Nemotron-4-340B-Instruct, Mixtral-8x22BInstruct-v0.1 und viele andere sehen hervorragende Darsteller. Allerdings weisen offene Modelle im Vergleich zu den proprietären Großmodellen GPT-4-Turbo in vielen Bereichen noch erhebliche Lücken auf. Zusätzlich zu allgemeinen Modellen wurden einige offene Modelle entwickelt, die sich auf Schlüsselbereiche spezialisieren, wie etwa DeepSeek-Coder-V2 für Programmierung und Mathematik und InternVL für visuelle Sprachaufgaben.
 Google AI gewann die Silbermedaille der IMO Mathematical Olympiad, das mathematische Argumentationsmodell AlphaProof wurde eingeführt und Reinforcement Learning ist zurück
Jul 26, 2024 pm 02:40 PM
Google AI gewann die Silbermedaille der IMO Mathematical Olympiad, das mathematische Argumentationsmodell AlphaProof wurde eingeführt und Reinforcement Learning ist zurück
Jul 26, 2024 pm 02:40 PM
Für KI ist die Mathematikolympiade kein Problem mehr. Am Donnerstag hat die künstliche Intelligenz von Google DeepMind eine Meisterleistung vollbracht: Sie nutzte KI, um meiner Meinung nach die eigentliche Frage der diesjährigen Internationalen Mathematikolympiade zu lösen, und war nur einen Schritt davon entfernt, die Goldmedaille zu gewinnen. Der IMO-Wettbewerb, der gerade letzte Woche zu Ende ging, hatte sechs Fragen zu Algebra, Kombinatorik, Geometrie und Zahlentheorie. Das von Google vorgeschlagene hybride KI-System beantwortete vier Fragen richtig und erzielte 28 Punkte und erreichte damit die Silbermedaillenstufe. Anfang dieses Monats hatte der UCLA-Professor Terence Tao gerade die KI-Mathematische Olympiade (AIMO Progress Award) mit einem Millionenpreis gefördert. Unerwarteterweise hatte sich das Niveau der KI-Problemlösung vor Juli auf dieses Niveau verbessert. Beantworten Sie die Fragen meiner Meinung nach gleichzeitig. Am schwierigsten ist es meiner Meinung nach, da sie die längste Geschichte, den größten Umfang und die negativsten Fragen haben
 PRO |. Warum verdienen große Modelle, die auf MoE basieren, mehr Aufmerksamkeit?
Aug 07, 2024 pm 07:08 PM
PRO |. Warum verdienen große Modelle, die auf MoE basieren, mehr Aufmerksamkeit?
Aug 07, 2024 pm 07:08 PM
Im Jahr 2023 entwickeln sich fast alle Bereiche der KI in beispielloser Geschwindigkeit weiter. Gleichzeitig verschiebt die KI ständig die technologischen Grenzen wichtiger Bereiche wie der verkörperten Intelligenz und des autonomen Fahrens. Wird der Status von Transformer als Mainstream-Architektur großer KI-Modelle durch den multimodalen Trend erschüttert? Warum ist die Erforschung großer Modelle auf Basis der MoE-Architektur (Mixture of Experts) zu einem neuen Trend in der Branche geworden? Können Large Vision Models (LVM) ein neuer Durchbruch im allgemeinen Sehvermögen sein? ...Aus dem PRO-Mitglieder-Newsletter 2023 dieser Website, der in den letzten sechs Monaten veröffentlicht wurde, haben wir 10 spezielle Interpretationen ausgewählt, die eine detaillierte Analyse der technologischen Trends und industriellen Veränderungen in den oben genannten Bereichen bieten, um Ihnen dabei zu helfen, Ihre Ziele in der Zukunft zu erreichen Jahr vorbereitet sein. Diese Interpretation stammt aus Week50 2023
 Um ein neues wissenschaftliches und komplexes Frage-Antwort-Benchmark- und Bewertungssystem für große Modelle bereitzustellen, haben UNSW, Argonne, die University of Chicago und andere Institutionen gemeinsam das SciQAG-Framework eingeführt
Jul 25, 2024 am 06:42 AM
Um ein neues wissenschaftliches und komplexes Frage-Antwort-Benchmark- und Bewertungssystem für große Modelle bereitzustellen, haben UNSW, Argonne, die University of Chicago und andere Institutionen gemeinsam das SciQAG-Framework eingeführt
Jul 25, 2024 am 06:42 AM
Herausgeber | Der Frage-Antwort-Datensatz (QA) von ScienceAI spielt eine entscheidende Rolle bei der Förderung der Forschung zur Verarbeitung natürlicher Sprache (NLP). Hochwertige QS-Datensätze können nicht nur zur Feinabstimmung von Modellen verwendet werden, sondern auch effektiv die Fähigkeiten großer Sprachmodelle (LLMs) bewerten, insbesondere die Fähigkeit, wissenschaftliche Erkenntnisse zu verstehen und zu begründen. Obwohl es derzeit viele wissenschaftliche QS-Datensätze aus den Bereichen Medizin, Chemie, Biologie und anderen Bereichen gibt, weisen diese Datensätze immer noch einige Mängel auf. Erstens ist das Datenformular relativ einfach, die meisten davon sind Multiple-Choice-Fragen. Sie sind leicht auszuwerten, schränken jedoch den Antwortauswahlbereich des Modells ein und können die Fähigkeit des Modells zur Beantwortung wissenschaftlicher Fragen nicht vollständig testen. Im Gegensatz dazu offene Fragen und Antworten
 Die Genauigkeitsrate erreicht 60,8 %. Das auf Transformer basierende Modell zur Vorhersage der chemischen Retrosynthese wurde in der Unterzeitschrift „Nature' veröffentlicht
Aug 06, 2024 pm 07:34 PM
Die Genauigkeitsrate erreicht 60,8 %. Das auf Transformer basierende Modell zur Vorhersage der chemischen Retrosynthese wurde in der Unterzeitschrift „Nature' veröffentlicht
Aug 06, 2024 pm 07:34 PM
Herausgeber | KX-Retrosynthese ist eine entscheidende Aufgabe in der Arzneimittelforschung und organischen Synthese, und KI wird zunehmend eingesetzt, um den Prozess zu beschleunigen. Bestehende KI-Methoden weisen eine unbefriedigende Leistung und eine begrenzte Vielfalt auf. In der Praxis verursachen chemische Reaktionen häufig lokale molekulare Veränderungen mit erheblichen Überschneidungen zwischen Reaktanten und Produkten. Davon inspiriert schlug das Team von Hou Tingjun an der Zhejiang-Universität vor, die einstufige retrosynthetische Vorhersage als eine Aufgabe zur Bearbeitung molekularer Ketten neu zu definieren und dabei die Zielmolekülkette iterativ zu verfeinern, um Vorläuferverbindungen zu erzeugen. Außerdem wird ein bearbeitungsbasiertes retrosynthetisches Modell EditRetro vorgeschlagen, mit dem qualitativ hochwertige und vielfältige Vorhersagen erzielt werden können. Umfangreiche Experimente zeigen, dass das Modell beim Standard-Benchmark-Datensatz USPTO-50 K eine hervorragende Leistung mit einer Top-1-Genauigkeit von 60,8 % erzielt.